91e Congrès de l'Acfas
Auteur et co-auteurs
Université du Québec à Montréal
Commentaires
Carolane
Veilleux
J'aimerais simplement…
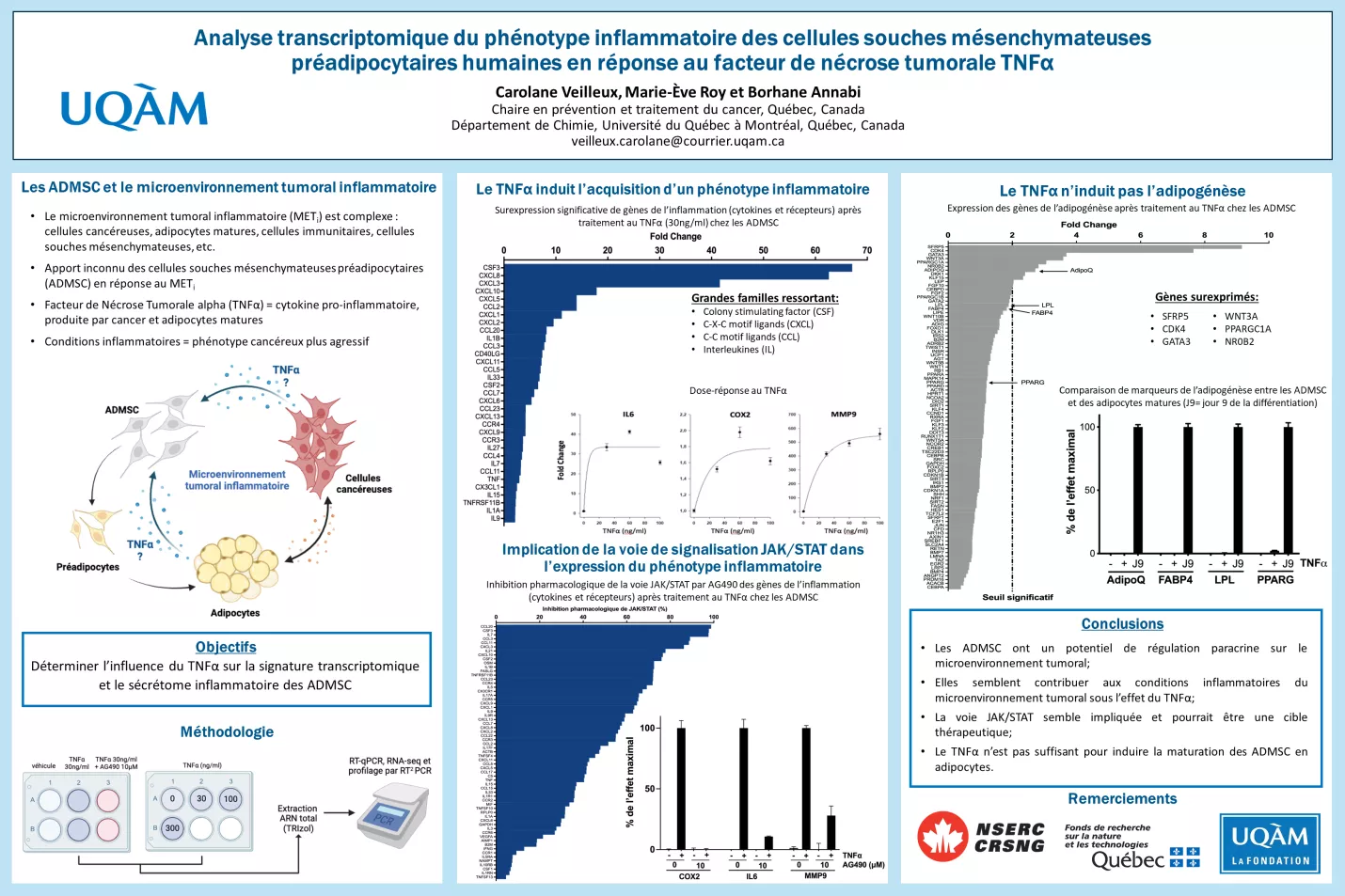
J'aimerais simplement spécifier que les résultats préliminaires, au temps de l'écriture du résumé, semblaient indiquer la surexpression de marqueurs de l'adipogénèse (FABP4, LPL, PPARG et AdipoQ). Toutefois, il s'agissait de signaux non spécifiques. Les résultats et validations subséquentes ont confirmé que l'adipogénèse n'était pas induite par l'action du TNFa.